试想一下,将药品序列化合规性与冷链监控联系起来,会带来怎样的质量优势?

自 DSCSA(药品供应链安全法案)出台并获得国会和参议院批准以来,在国际标准拥护者 GS1 的帮助下,为确保美国和全球完全遵守该法案,各方一直在共同努力。
目前,完全合规和准备就绪的日期已确定为 2023 年 11 月 27 日,这正是考虑通过合并 DSCSA 和冷链法规对高价值疫苗、制药药品和生物制剂进行温度监控,将质量、安全和合规性提升到一个新水平的大好时机。
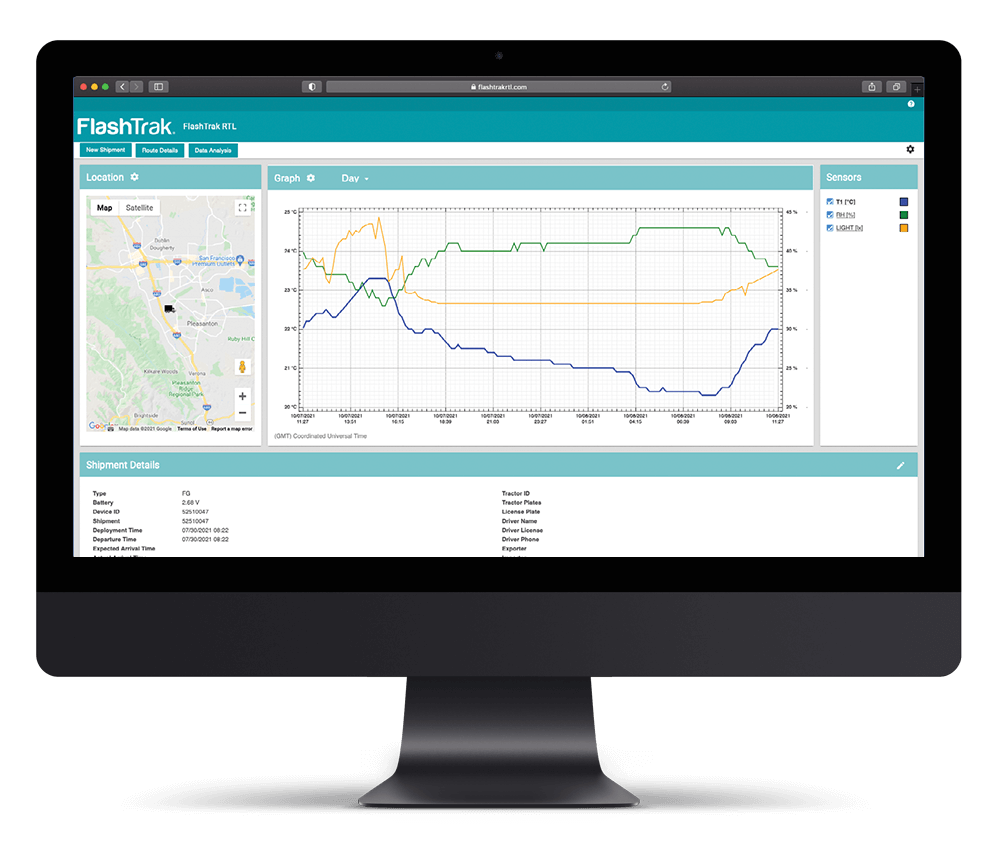
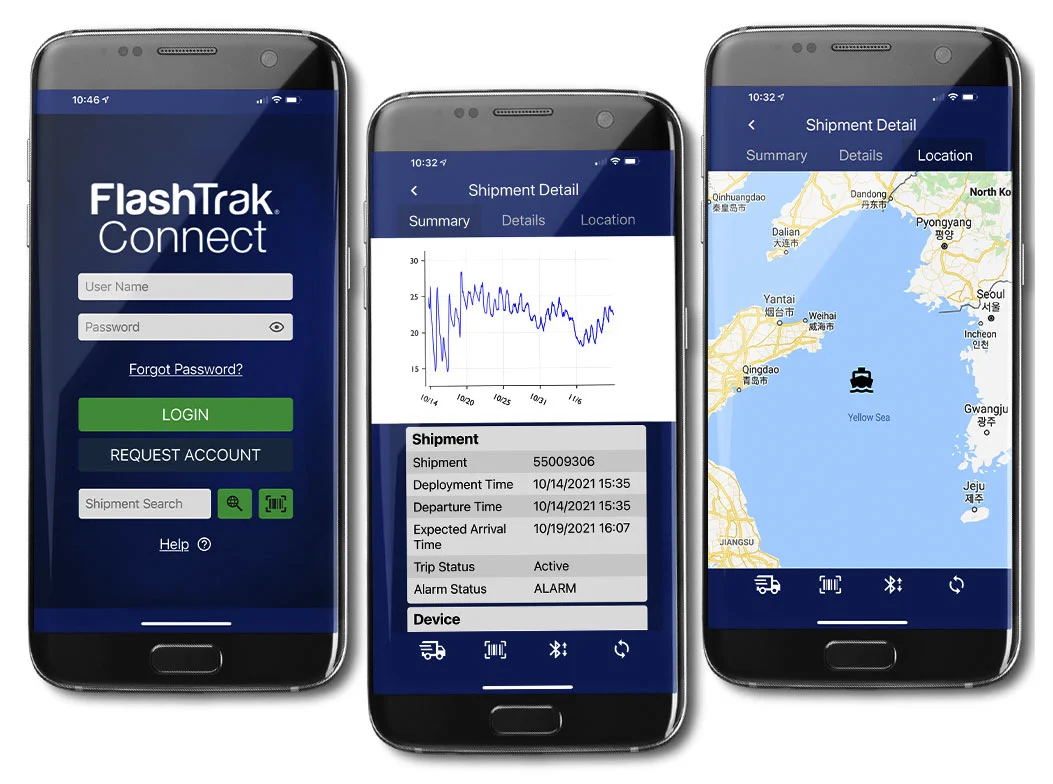
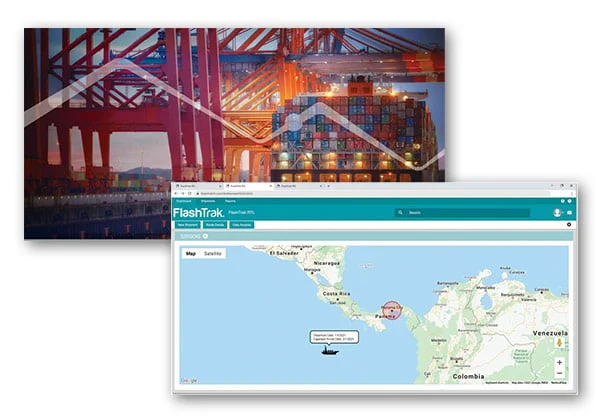
大多数需要符合 DSCSA 要求的药品生产商在很多情况下都已经建立了冷链产品的温度监控和管理系统,并建立了从货物出库到到达目的地的最低正确温度和条件检查应用程序。除此以外,许多公司现在还采用了实时跟踪和温度监控技术,因此,如果出现偏差,完全有可能采取纠正措施,防止货物全部丢失。后一种跟踪方法在大多数情况下都配有云服务,这样物流人员就能知道产品在哪里,在运输过程中发生了什么。
因此,现在可能有两个数据库,其中包含与可能直接影响高价值药物相关产品在供应链中的疗效、安全性和合规性的事件相关的宝贵数据。然而,目前这两组数据都是独一无二的,各自独立,因此,如果只关注一个数据链,就可能会忽略合规数据。
尽管大多数公司正在迅速接近或已经符合 DSCSA 法规,但在此之前的许多年里,他们一直在跟踪和监控冷链产品的温度合规性,因此这项活动并不新鲜。不过,现在也许是进一步研究是否有机会建立一个将这两种数据流汇集在一起的单一来源点的好时机。这将有助于确保序列化和冷链数据的全面合规性,从而保证交付给患者的不仅是非假冒产品,而且在必要时还对温度限制进行了监控,以确保药效和稳定性水平,从而保证患者的全面安全和利益。